Leventa® 1 mg/ml
Lösung zum Eingeben für Hunde
Zusammensetzung
Jeder ml enthält:
Wirkstoffe:
Levothyroxin-Natrium (als Multihydrat) 1 mg
(entsprechend 0,97 mg Levothyroxin)
Sonstige Bestandteile:
Ethanol 96 % 0,15 ml
Klare, farblose bis leicht rötlich gefärbte Lösung.
Zieltierart(en)
Hund
Anwendungsgebiete
Zur Behandlung der Hypothyreose bei Hunden.
Gegenanzeigen
Nicht anwenden bei Hunden mit Hyperthyreose oder mit unbehandelter Nebenniereninsuffizienz (Hypoadrenokortizismus).
Nicht anwenden bei Überempfindlichkeit gegen den Wirkstoff oder einen der sonstigen Bestandteile.
Besondere Warnhinweise
Besondere Vorsichtsmaßnahmen für die sichere Anwendung bei den Zieltierarten:
Das Tierarzneimittel sollte bei Hunden mit Herzerkrankungen, Diabetes mellitus oder behandelter Nebenniereninsuffizienz (Hypoadrenokortizismus) unter Vorsicht angewendet werden. Für solche Hunde empfiehlt sich, die Levothyroxin-Therapie stufenweise einzuleiten. Es sollte mit 25 % der normalen Dosis begonnen werden, die in Abständen von vierzehn Tagen um jeweils 25 % erhöht wird, bis eine optimale Stabilisierung erreicht ist.
Die klinische Diagnose Hypothyreose sollte mit Hilfe geeigneter labordiagnostischer Methoden bestätigt werden.
Besondere Vorsichtsmaßnahmen für den Anwender:
Bei versehentlicher Einnahme ist unverzüglich ein Arzt zu Rate zu ziehen und die Packungsbeilage oder das Etikett vorzuzeigen.
Zur Beachtung: Dieses Tierarzneimittel enthält eine hohe Konzentration an L-Thyroxin-Natrium und kann bei Aufnahme ein Risiko für den Menschen darstellen.
Nach der Anwendung Hände waschen.
Bei Benetzung der Augen umgehend mit Wasser spülen.
Trächtigkeit und Laktation:
Die Verträglichkeit der Anwendung bei trächtigen Hündinnen wurde nicht untersucht.
Thyroxin ist jedoch essenziell für die normale fötale Entwicklung. Eine Hypothyreose während der Trächtigkeit kann möglicherweise zu einer eingeschränkten Entwicklung kognitiver Fähigkeiten sowie zu einer erhöhten fötalen Mortalität führen. Während der Trächtigkeit kann der maternale Bedarf an Schilddrüsenhormonen erhöht sein. Trächtige Hündinnen unter Behandlung sollten deshalb vom Deckungstermin bis mehrere Wochen nach dem Werfen regelmäßig überwacht werden, da sich die erforderliche Dosis während der Trächtigkeit und Laktation ändern kann.
Zur Anwendung bei laktierenden Hündinnen oder bei zur Zucht vorgesehenen Hunden liegen keine Erfahrungen vor.
Wechselwirkung mit anderen Arzneimitteln und sonstige Wechselwirkungen:
Die Resorption von L-Thyroxin kann bei gleichzeitiger Anwendung von Antazida wie Aluminium- oder Magnesiumsalzen, Kalziumcarbonat, Eisensulfat oder Sucralfat verringert sein. Deshalb sollte die gleichzeitige Anwendung des Tierarzneimittels mit den oben genannten Wirkstoffen vermieden werden. Zwischen der Anwendung des Tierarzneimittels und diesen Stoffen sollten mindestens zwei Stunden Abstand liegen.
Die therapeutische Wirkung des Tierarzneimittels kann durch alle Substanzen, die den Stoffwechsel oder die Verteilung von Schilddrüsenhormonen beeinflussen, verändert sein (z.B. Tierarzneimittel, die Proteinbindungsstellen besetzen, die die Konzentration an thyroxinbindendem Globulin im Serum, den hepatischen Thyroxinabbau oder den peripheren Umbau von Thyroxin in Triiodthyronin beeinflussen). Deshalb wird empfohlen, bei gleichzeitiger Anwendung des Tierarzneimittels mit Tierarzneimitteln, die eine der oben genannten Eigenschaften aufweisen, wiederholt zu prüfen, ob die Schilddrüsenhormonkonzentration ausreichend ist, und ggf. die Dosis des Tierarzneimittels anzupassen.
Umgekehrt kann die Verabreichung von L-Thyroxin auch die Pharmakokinetik und Wirksamkeit anderer zeitgleicher Therapien beeinflussen. Bei mit Insulin behandelten diabetischen Hunden, kann die Substitution mit L-Thyroxin den Insulinbedarf verändern. Bei herzinsuffizienten Hunden kann die therapeutische Wirkung von Herzglykosiden durch eine Substitution mit L-Thyroxin verringert sein. Deshalb sollten Hunde, die mit einem dieser Tierarzneimittel behandelt werden, zu Beginn einer Behandlung mit diesem Tierarzneimittel sorgfältig überwacht werden.
Bitte informieren Sie ihren Tierarzt, wenn ihr Hund vor oder während der Behandlung mit diesem Tierarzneimittel auch andere Tierarzneimittel erhält.
Überdosierung:
Die klinischen Symptome einer Überdosierung mit L-Thyroxin entsprechen denen einer Hyperthyreose und umfassen Gewichtsverlust, Hyperaktivität, Tachykardie, Polydipsie, Polyurie, Polyphagie und Diarrhoe. Diese Symptome sind in der Regel leicht und vollständig reversibel. Eine Überdosierung kann auch mit reversiblen Änderungen von Blutwerten einhergehen wie erhöhten Werten an Glukose und anorganischem Phosphor, einem erhöhten Albumin-Globulin-Verhältnis sowie erniedrigten Gesamtprotein- und Cholesterinwerten.
In einer Verträglichkeitsstudie mit gesunden Hunden, die über 91 Tage mit diesem Tierarzneimittel in einer täglichen Dosis von 40 µg/kg Körpergewicht behandelt wurden, zeigten sich keinerlei relevanten klinischen Symptome. Bei Dosierungen von 120 und 200 µg/kg Körpergewicht traten bei den Hunden keine anderen Symptome als die einer Hyperthyreose, hauptsächlich Gewichtsverlust, auf. Diese Symptome waren leicht, reversibel und verschwanden innerhalb von 5 Wochen nach Behandlungsende.
Um nicht-resorbierte Anteile des Tierarzneimittels aus dem Gastrointestinaltrakt zu entfernen, sollten die üblichen Maßnahmen eingeleitet werden.
Bei Verdacht einer chronischen Überdosierung sollte die Dosis neu festgelegt werden.
Wesentliche Inkompatibilitäten:
Keine bekannt.
Nebenwirkungen
Hund:
| Selten (1 bis 10 Tiere / 10 000 behandelte Tiere): | Gewichtsverlust, Polydipsie (gesteigerter Durst) Polyurie (vermehrter Harnabsatz) Hyperaktivität Erbrechen, Diarrhoe. |
| Sehr selten (< 1 Tier / 10 000 behandelte Tiere, einschließlich Einzelfallberichte): | Polyphagie (verstärkter Hunger) Tachykardie (erhöhte Herzfrequenz) Hautreaktion (z. B. Schuppen1)2 |
1 Milde bis mäßige Ausprägung.
2 Vorübergehend und selbstauflösend.
Nebenwirkungen in Zusammenhang mit einer L-Thyroxin-Natrium-Behandlung entsprechen überwiegend denen einer Hyperthyreose (Schilddrüsenüberfunktion) und entstehen meist durch Überdosierung bei der Therapie.
Die Meldung von Nebenwirkungen ist wichtig. Sie ermöglicht die kontinuierliche Überwachung der Verträglichkeit eines Tierarzneimittels. Falls Sie Nebenwirkungen, insbesondere solche, die nicht in der Packungsbeilage aufgeführt sind, bei Ihrem Tier feststellen oder falls Sie vermuten, dass das Tierarzneimittel nicht gewirkt hat, teilen Sie dies bitte zuerst Ihrem Tierarzt mit. Sie können Nebenwirkungen auch an den Zulassungsinhaber unter Verwendung der Kontaktdaten am Ende dieser Packungsbeilage oder über Ihr nationales Meldesystem melden.
Dosierung für jede Tierart, Art und Dauer der Anwendung
Zum Eingeben.
Bei einer Schilddrüsenhormon-Substitutionstherapie mit L-Thyroxin sind Dosis und Behandlungsschema individuell für jeden Hund einzustellen. Die empfohlene Anfangsdosis beträgt 20 μg L-Thyroxin-Natrium/kg Körpergewicht einmal täglich. Dies entspricht 0,2 ml des Tierarzneimittels pro 10 kg Körpergewicht.
Nach 4 Wochen Behandlung sollte eine Dosisanpassung basierend auf den Ergebnissen der klinischen Untersuchung sowie auf der 4-6 Stunden nach Verabreichung ermittelten Schilddrüsenhormonkonzentration erfolgen. Weitere Bestimmungen des Hormonstatus und Dosisanpassungen können, sofern erforderlich, alle 4 Wochen erfolgen.
Eine Erhaltungsdosis im Bereich von 10 bis 40 µg/kg Körpergewicht einmal täglich ist in der Regel ausreichend. Die geeignete Dosis für ihren Hund wird von ihrem Tierarzt festgelegt. Abhängig von der Dosis und dem Körpergewicht ihres Hundes kann das täglich zu verabreichende Volumen (in ml) des Tierarzneimittels anhand nachfolgender Tabelle ermittelt werden:
| Körpergewicht (kg) | Dosierung (Mikrogramm/kg) | |||
| 10 | 20 | 30 | 40 | |
| Volumen des Tierarzneimittels (ml) | ||||
| 5 | 0.05 | 0.10 | 0.15 | 0.20 |
| 10 | 0.10 | 0.20 | 0.30 | 0.40 |
| 15 | 0.15 | 0.30 | 0.45 | 0.60 |
| 20 | 0.20 | 0.40 | 0.60 | 0.80 |
| 25 | 0.25 | 0.50 | 0.75 | 1.00 |
| 30 | 0.30 | 0.60 | 0.90 | 1.20 |
| 35 | 0.35 | 0.70 | 1.05 | 1.40 |
| 40 | 0.40 | 0.80 | 1.20 | 1.60 |
| 45 | 0.45 | 0.90 | 1.35 | 1.80 |
| 50 | 0.50 | 1.00 | 1.50 | 2.00 |
Die Dosis für Hunde mit einem Körpergewicht von über 50 kg sollte in gleicher Weise wie in der Tabelle ermittelt werden.
Sind eine geeignete Dosis und ein geeignetes Behandlungsschema festgelegt, wird eine Überprüfung der Schilddrüsenhormonkonzentration alle 6 Monate empfohlen.
Metabolische Symptome wie Lethargie bessern sich in der Regel innerhalb von 2 Wochen nach Behandlungsbeginn, während Haut- und Fellveränderungen erst nach 6-wöchiger oder noch längerer Behandlung eine Verbesserung erfahren.
Hinweise für die richtige Anwendung
Das Tierarzneimittel sollte immer zur gleichen Tageszeit verabreicht werden. Die Resorption von L-Thyroxin wird durch Fütterung beeinflusst. Daher sollte L-Thyroxin bevorzugt immer 2 bis 3 Stunden vor der Fütterung verabreicht werden. Andernfalls sollte stets die gleiche Futterart und –menge gefüttert werden.
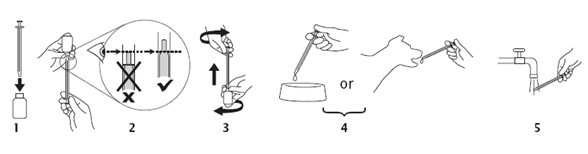
Hinweise zum Gebrauch der Spritze zum Eingeben:
Die Flasche öffnen. (1) Die Dosierspritze mit sanftem Druck auf die Öffnung der Flasche setzen. (2) Die Flasche mit der verbundenen Spritze umdrehen und die Lösung durch Ziehen des Spritzenstempels so weit in die Spritze ziehen, bis das Ende des Stempels an der Markierung für das gewünschte Volumen bzw. Körpergewicht steht. (3) Flasche mit Spritze wieder umdrehen und die Spritze abnehmen. (4) Nach Verabreichung des Tierarzneimittels die (5) Spritze mit sauberem Wasser reinigen und lufttrocknen lassen.
Wartezeiten
Nicht zutreffend.
Besondere Lagerungshinweise
Außerhalb der Sicht und Reichweite von Kindern aufbewahren.
Im Kühlschrank lagern (2 °C – 8 °C). In der Originalverpackung aufbewahren.
Haltbarkeit nach dem ersten Öffnen/Anbruch der Primärverpackung: 6 Monate.
Sie dürfen dieses Tierarzneimittel nach dem auf dem Etikett angegebenen Verfalldatum nach „Exp.“ nicht mehr anwenden. Das Verfalldatum bezieht sich auf den letzten Tag des Monats.
Besondere Vorsichtsmaßnahmen für die Entsorgung
Nicht aufgebrauchte Tierarzneimittel sind vorzugsweise bei Schadstoffsammelstellen abzugeben. Bei gemeinsamer Entsorgung mit dem Hausmüll ist sicherzustellen, dass kein missbräuchlicher Zugriff auf diese Abfälle erfolgen kann. Tierarzneimittel dürfen nicht mit dem Abwasser bzw. über die Kanalisation entsorgt werden.
Nutzen Sie Rücknahmesysteme für die Entsorgung nicht verwendeter Tierarzneimittel oder daraus entstandener Abfälle nach den örtlichen Vorschriften und die für das betreffende Tierarzneimittel geltenden nationalen Sammelsysteme.
Diese Maßnahmen dienen dem Umweltschutz.
Fragen Sie Ihren Tierarzt oder Apotheker, wie nicht mehr benötigte Arzneimittel zu entsorgen sind.
Einstufung von Tierarzneimitteln
Tierarzneimittel, das der Verschreibungspflicht unterliegt.
Zulassungsnummern und Packungsgrößen
Zul.-Nr. 400937.00.00
Faltschachtel mit einer 30-ml-Flasche und einer 1-ml-Dosierspritze
Faltschachtel mit sechs 30-ml-Flaschen und sechs 1-ml-Dosierspritzen
Faltschachtel mit zwölf 30-ml-Flaschen und zwölf 1-ml-Dosierspritzen
Es werden möglicherweise nicht alle Packungsgrößen in Verkehr gebracht.
Datum der letzten Überarbeitung der Packungsbeilage
06/2025
Detaillierte Angaben zu diesem Tierarzneimittel sind in der Produktdatenbank der Europäischen Union verfügbar (https://medicines.health.europa.eu/veterinary).
Verschreibungspflichtig
